CO2再利用合成化學品單體的觸媒技術
- 刊登日期:2022-10-25
- 資料來源:工研院材化所
- 作者:許希彥、楊智堯、吳國卿
CO2再利用合成化學品單體的觸媒技術
The catalytic technologies for CO2 utilization on preparing chemical monomers
許希彥H.Y. Hsu1、楊智堯C.Y. Yang2、吳國卿K.C. Wu3
工研院材化所(ITRI/MCL) 先進觸媒研究室1經理、2副研究員、3資深研究員
摘要:
以二氧化碳當作原料製作碳酸二烷基酯與2,5-呋喃二甲酸(FDCA)之觸媒技術近年已有重要的發展。碳酸二烷基酯可應用生產聚碳酸酯(PC)、異氰酸酯、聚碳酸酯二醇等化學品,為應用廣泛的原料單體。而2,5-呋喃二甲酸可做為生質單體,其聚合成的PEF聚酯材料比現有PET聚酯材料對二氧化碳及氧氣具有優異的阻氣性及更高的機械強度,此二項單體的觸媒技術開發都朝向高效率催化、環境無害、低成本能耗等方向發展,未來都是以CO2料源製造關鍵化學單體的潛力產品。
The catalytic technologies have made encouraging progress on preparing chemical monomers such as dialkyl carbonate and 2,5-furandicarboxylic acid (FDCA) using carbon dioxide as a raw material in recent years. Dialkyl carbonate is a widely used monomer in producing polycarbonate (PC), isocyanate, polyurethane, polycarbonate diol and other chemicals. 2,5-furandicarboxylic acid (FDCA) can be used as a monomer from renewable biomass. The PEF polyester from FDCA monomer observed superior gas barrier to carbon dioxide and oxygen and higher mechanical strength than commercial PET polyester. These two monomers developing toward high-efficiency, environmental friendly process and lower energy consumption from CO2 sources will be manufactured in the future.
關鍵詞/Key words
CO2再利用(CO2 Utilization)、碳酸二烷基酯(Dialkyl Carbonate)、羧基化反應(Carboxylation)
一、前言:
因應全球的CO2減碳趨勢,以CO2為原料開發具有經濟效益的關鍵化學品,應用於塑化材料,將對我國相關碳排放產業帶來新發展契機。然而CO2分子為熱力學上穩定的分子,不易與其它原料進行反應,全球化工產業皆在積極尋求有效的觸媒系統可將CO2在較低的反應條件下做有效的轉化應用。在近年研發中,有些CO2的催化反應可透過觸媒的改善而逐步邁入可商業化的階段,例如(1)CO2在觸媒催化下,進行酯化反應形成碳酸酯類的化合物或直接合成高分子聚合物, (2) CO2與苯環或烯炔類進行加成反應形成含有羧酸官能基的化學中間體。若能對此兩類反應儘速投入相關技術研發佈局,將有可能建立以CO2為料源的塑化單體材料新產業。
二、CO2合成碳酸二烷基酯(DRC)
碳酸酯類化合物包含單分子的二烷基酯(dialkyl carbonate, DRC)類的化合物及碳酸酯類聚合物。其中單分子的碳酸二烷基酯是化工產業使用的基礎化學品。包含碳酸二甲酯(DMC),碳酸二乙酯(DEC),碳酸二辛酯(DOC),碳酸二苯酯(DPC)等多項有用的碳酸二烷基類化合物。其中以碳酸二甲酯的需求量最高,預估全球每年可達50萬噸需求量。而此類碳酸二烷基酯可應用領域為(1)做為甲基化、乙基化或羰基化等反應試劑,(2)應用生產聚碳酸酯(PC)、異氰酸酯、聚氨基甲酸酯、聚碳酸酯二醇等化學品。(3) 可和雙醇單體合成聚合物,具有特殊物性的聚碳酸酯二醇(Polycarbonate diols,PCDL),可應用於PU及聚酯產業。(4)做為無毒的綠色環保溶劑(如碳酸二甲酯、碳酸丙烯酯),與大多有機物具有優良的溶解性能、黏度低、介電常數小及表面張力大等特質,可用於塗料、化學合成、清潔用等溶劑。(5)用於汽油添加劑,可提高汽油中的高辛烷值作用,降低汽車廢氣總排放量,及不溶於水、低毒和快速生物分解性等性質,(6) 隨著電動車的發展,在鋰電池中作為電解液使用。(7)做為化妝品及個人護理用之配方助劑,碳酸二辛酯主要做為膚感乾爽的新型潤膚劑。
其中碳酸二甲酯(DMC)是分子量最小的碳酸酯類化合物。傳統生產DMC的方法是採用含有劇毒的光氣原料法,反應快速且光氣成本低,可大量生產。但因光氣為劇毒化學品,且伴隨產生大量氯化鈉副產物,對設備造成腐蝕及增加廢棄物處理的費用,因應環保要求而逐漸減少使用。目前工業界最常用的製程方法是以CO和甲醇進行氧化反應而生成DMC,但目前CO仍來自於煤、天然氣等石化原料,無法提供有效的CO2減量效果。而以CO2為料源製備DMC的方法早在2000年即為東聯化工與奇美公司合作所採用的生產方法。先以CO2與環氧乙烷(Ethylene oxide, EO)反應合成碳酸乙烯酯(Ethylene carbonate, EC),EC再和甲醇進行酯交換反應生成DMC,而後轉成DPC及生產PC聚合物。此製程從2000年開始即每年使用3萬噸的CO2產製PC產品。適用於有EO原料的廠商,製程會伴隨產生乙二醇副產物可做其它衍生應用,此製程為早期使用CO2開發的優良環保製程。(圖一)
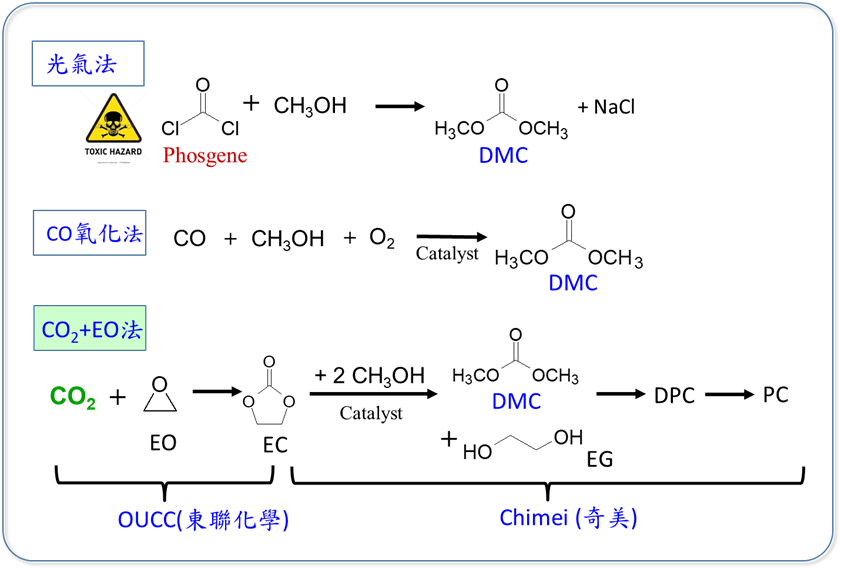
圖一、合成碳酸二甲酯-商業化製程技術
近年在學界以CO2加上甲醇直接合成DMC蔚為風潮。由於CO2加上甲醇進行酯化脫水形成DMC的反應為平衡反應,其吉布斯自由能(Gibbs free energy)為+26KJ/mol,因此採用正常反應條件是不利於DMC的生成,其理論產率約在1-2%。(圖二)。經過不斷改善各種可能的觸媒系統,發現以氧化鈰CeO2 和氧化鋯ZrO2為主要成份是較佳的觸媒系統。其衍生觸媒系統包含將磷酸放在ZrO2載體上,或是將CeO2放在氧化鋁載體,也可有效提升反應速率。也有文獻表示不同的晶體型態也有催化效果,奈米線CeO2的產率優於一般粉體型的CeO2。因此奈米線存在某些特定的晶面對CO2的吸附及轉換是有助益的,CO2若是吸附在CeO2上形成bidentate carbonate則被認為是有高活性的吸附。(圖三)
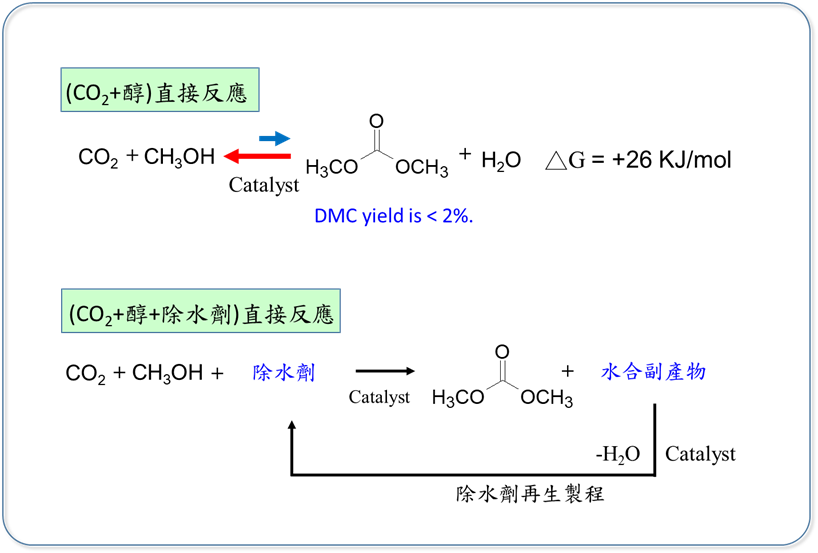
圖二、合成碳酸二甲酯-發展中的新製程技術

圖三、CeO2觸媒可能的CO2吸附態
由於CO2直接加甲醇合成DMC的平衡產率過低,若能打破平衡方式,將副產物(水)移除,將能使平衡傾向DMC的產率增加。一般酯化反應是用溶劑共沸法將副產物(水)移除,但由於CO2為氣體無法使用此法,因此改為使用易與水反應的除水劑摻在反應中,當反應中有水出現時,除水劑即時與水反應而使DMC大量保存在產物端。一般化學反應常用的除水試劑有orthoesters、epoxide、ketal(acetal)、ether、nitrile等。其中以orthoesters、epoxide反應較佳,但價格較貴且無法再生,因此無法用於大量生產。使用上述除水劑的一般反應DMC產率皆在16%以下。若是使用分子篩進行物理性吸附水分子,測試結果DMC的產率約只有3-4%(表一)。而日本東北大學Tomeshige 教授在實驗室中使用2-cyanopyridine進行反應時,可以有明顯的反應性,在12個小時的反應時間,DMC可以大於90%以上的產率,明顯的優於過往的各種除水劑。不過2-cyanopyridine目前要再生仍不容易,不易被大量使用,仍需要解決此項再生問題。(表二)
表一、CO2與甲醇反應-使用多種除水劑合成DMC
| 觸媒 | 反應壓力 (bar) |
反應溫度 (℃) |
反應時間(hr) | 除水劑 | 除水劑 (mole) |
產率DMC (%) |
| CeO2(ITRI-5)a | 40 | 110 | 24 | Acetonitrile | 1 | 0.23% |
| CeO2(ITRI-5) | 40 | 110 | 24 | Diethyl ether | 0.5 | 0.27% |
| CeO2(ITRI-5) | 40 | 110 | 24 | Dimethoxypropane | 0.6 | 6.74% |
| CeO2(ITRI-5) | 40 | 110 | 24 | 3A zeolite | 50g | 3.69% |
| CeO2/4Ab | 60 | 120 | - | 4A zeolite | - | 3.23% |
| CeO2c | 50 | 110 | 90 | Dimethoxypropane | 0.01 | 1.20% |
a:工研院自製觸媒CeO2(ITRI-5)
b: Journal of Cleaner Production 103 (2015) 847-853
c: Appl. Catal. A:General, 237 (2002) 103-109
表二、CO2與甲醇反應-使用2-cyanopyridine除水劑合成DMC
| 觸媒 | 反應壓力( bar) | 反應溫度(℃) | 反應時間(hr) | 觸媒 (g) |
MeOH (mole) |
除水劑 (mole) |
產率DMC (%) |
| CeO2(ITRI-5)a | 40 | 110 | 24 | 6 | 1 | 0.5 | 80.40% |
| CeO2(ITRI-7)b | 40 | 110 | 24 | 6 | 1 | 0.5 | 91.17% |
| CeO2c | 50 | 110 | 16 | 0.34 | 0.02 | 0.1 | 94.00% |
除水劑:2-cyanopyridine, a,b: 工研院自製觸媒CeO2(ITRI-5), CeO2(ITRI-7)
*Catal. Lett., 76 (2001) 71-74.
目前旭化成(Asahi)公司直接將CO2和烷基醇反應轉換成碳酸二烷基酯的方法為具有工業化開發潛力的技術,其製程是選用錫觸媒做為催化劑又附有除水劑的功能,此類二烷基錫氧化物為酯化反應常用的催化劑,使用在合成碳酸酯反應、酯交換反應、合成有機矽聚合物、聚氨酯固化反應等。其合成DRC的方法是以三步法進行循環反應。第一步是以二烷基錫氧化物與一級醇進行脫水反應,從反應溶液中去除低沸點成分的水,得到四烷基二錫氧烷的催化劑中間物。第二步是四烷基二錫氧烷再與一級醇進行第二次的脫水反應生成具有活性的二烷基錫二醇鹽催化劑。第三步將二烷基錫二醇鹽通入二氧化碳,反應溫度在100-160℃,反應壓力在20-60bar,即可以生成DRC碳酸酯,以蒸餾方式獲得DRC產物,而觸媒吸水後轉變成中間物四烷基二錫氧烷,將此中間物再送回第二步的加醇脫水後,即可進入重覆循環回用。在整個製程中只有使用原料CO2、醇類及錫催化劑,產物為DRC碳酸酯、副產物為水,沒有發現其它的副產物,是為一項具有環保的製程。目前旭化成公司已將此法進行試量產測試。(圖四)
工研院近年在此項製程技術也開發出新的觸媒,在測試以CO2合成二丁基碳酸酯(dibutylcarbonate, DBC)及二己基碳酸酯(dihexylcarbonate, DHC)皆可提升產率。(1)在以CO2與正丁醇進行酯化反應合成DBC,傳統Sn觸媒產率為11-13%,而新觸媒則可以提升產率,經過10批次的反應,其產率皆維持在14-16%,觸媒保有相當穩定性。由於正丁醇的含水量較高,因此在做前兩段脫水反應時不容易將水分子帶出。造成脫水時需要使用較高量的正丁醇比例進行脫水反應,才能形成有活性的二烷基錫二醇鹽與CO2反應,因此單次的反應產率約在14-16%。其未反應的觸媒或丁醇皆可回收再循環進行反應。(2) 在以CO2與正己醇進行酯化反應合成DHC,使用工研院開發的觸媒,其產率可達DHC產率22%。並經過5批次的反應,觸媒保有相當穩定性。由於正己醇的含水量比正丁醇低,觸媒較易活化脫水,因此單次反應的DHC產率高於DBC。(圖五、圖六)
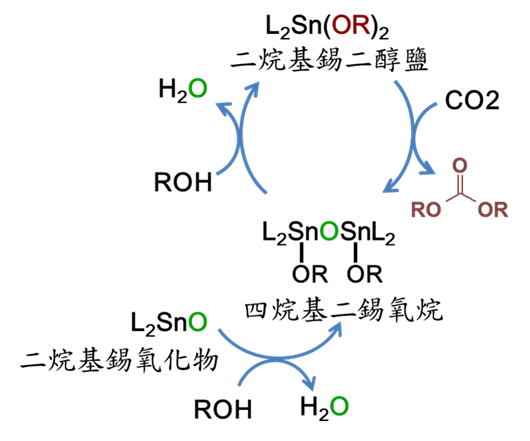
圖四、 旭化成公司開發的CO2和烷基醇反應轉換成DRC技術
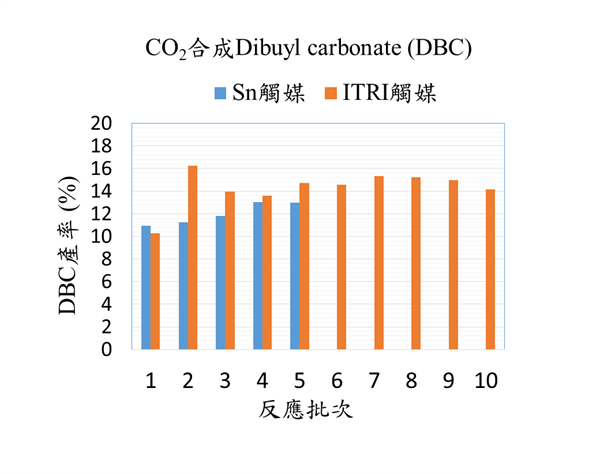
圖五、 Sn觸媒與工研院觸媒進行DBC加成反應測試
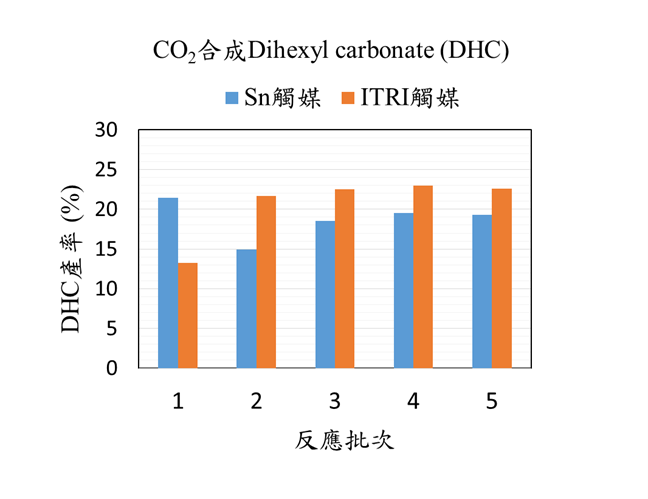
圖六、 Sn觸媒與工研院觸媒進行DHC加成反應測試
三、CO2羧基化反應
CO2為一個親電型分子(electrophile),可與苯酚或含多鍵型的分子進行羧基化反應,在分子結構加上羧酸官能基。傳統化工產業中使用CO2及苯酚製備水楊酸(2-Hydroxybenzoic acid)。其製程是使用鹼金族的鈉或鉀的氫氧化物,在8bar以下CO2及140-170℃合成水楊酸鹽,再加酸液酸化合成水楊酸(2-Hydroxybenzoic acid)。水楊酸是很多護膚品中的關鍵去角質成分,其酯類可以緩解關節和肌肉疼痛和消炎作用。而相似的製程也可合成出對位羧酸基的同分異構物-對羥基苯甲酸(p-Hydroxybenzoic acid, pHBA)。其製程也是將苯酚與氫氧化鉀(鈉)反應脫水形成酚鉀鹽後,通入5bar壓力以上的CO2,在較高的反應溫度220-230℃進行Kolbe-Schmitt加成轉位反應,再經加酸液後形成pHBA產物。pHBA被用作防腐劑、染色劑、農藥、可塑劑及做為工程塑膠的單體原料,搭配對苯二甲酸(Terephthalic Acid , TPA)、聯苯二酚(Biphenol)等其他單體,即可聚合出耐高溫達260~355℃的液晶聚合物(Liquid Crystal Polymer, LCP),應用於連接器(含外殼、接頭、底座等)及封裝基本材料。國內廠商已有三福化工及長春石化可以量產pHBA。
CO2羧基化反應最新的應用產品是以生質的糠醛化學品加上CO2製備出2,5-呋喃二甲酸化學品(2,5-furan dicarboxylic acid, FDCA)。根據美國2004年能源部的研究報告”Top Value Chemicals from Biomass : Volume I -- Results of Screening for Potential Candidates from Sugars and Synthesis Gas”,2,5-呋喃二甲酸為未來綠色生質的重要優選化學品之一,其主要應用是在聚酯材料。現有聚酯類商品中,以PET取酯材料應用產量最大,產品廣泛應用於化學纖維、電子、建築等各個產業。然而製備PET需使用對苯二甲酸(PTA)及乙二醇,早期皆來自石油及天然氣料源而無法減少CO2的排放。目前經由生質醱酵的酒精可以做成生質的乙二醇單體,但PTA雙羧酸單體仍是由石化製程生產,兩個單體聚合而成的PET成份中,生質成份小於30%。全球每年PET需求量約在2300萬噸以上,若能找到100%來自生質或CO2碳源的聚酯材料,就可以有效的減少CO2的排放量。而2,5-呋喃二甲酸與乙二醇聚合而成的PEF (polyethylene furandicarboxylate)材料是目前最能取代PET的潛力商品,此外FDCA還可以作為聚醯胺、藥品、增塑劑等化學品的原料。
2,5-呋喃二甲酸製造的PEF材料除了具有生質需求優勢外,在與PET性質比較上更有多項的優異性。PEF對二氧化碳、氧氣及水氣表現出更優異的阻氣性,其更高的機械強度也可生產出膜厚更薄的包裝材,進而減少薄膜與瓶子的包裝重量,適合應用於阻氣類的食品包裝材,延長食品的保存期限。同時,PEF由生質再生資源製作,與PET相比,PEF能減少50~70%的二氧化碳排放量,其材料有利於回收及降解,是相對於環境友善的產品。(表三)
表三、 PEF與PET聚酯材料性質比較
| PEF | PET | ||
| 阻氣性 | 氧氣 | 6-10 x | 1 x |
| 二氧化碳 | 4-10 x | 1 x | |
| 水氣 | 2-3 x | 1 x | |
| 熱分析 | Tg (℃) | 85-88 | 74-79 |
| Tm (℃) | 210-235 | 234-270 | |
| 機械性 | 1.6 x | 1 x | |
| 屈服強度(MPa) | 90-100 | 50-60 | |
| 彈性模量(GPa) | 3.1-3.3 | 2.1-2.2 | |
| 晶化時間(min) | 20-30 | 2-3 | |
| 密度(g/cm3) | 1.43 | 1.36 | |
FDCA製備方法目前分成化學製備法及生物製備法。化學製備法根據起始原料的不同,主要分為以下四大類:(1)以5-羥甲基糠醛(HMF)為原料經過氧化反應製備合成;(2)以糠酸或糠醛為原料,經過氧化及CO2羧基化反應製備;(3)以己糖二酸為原料,經過脫水製程合成;(4)以二甘醇酸及乙二醛為原料進行加成反應製備合成。生物製備法主要以HMF為原料,與化學製備法相比,生物製備法反應條件溫和、對環境相對無害等優勢,但其純化製程複雜,HMF原料具有細胞毒性等問題皆需要進一步的發展。(圖七)
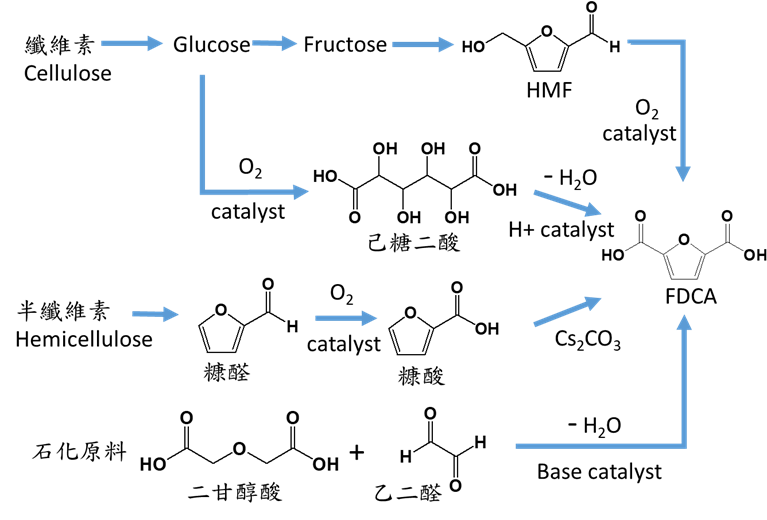
圖七、 以化學法製備FDCA單體的技術
近年來以5-羥甲基糠醛(HMF)為原料製備2,5-呋喃二甲酸的製程已由荷蘭的Avantium公司及瑞典Stora Enso公司進入試量產放大的階段。而2016年來自Standford大學的Kanan 教授使用糠醛先進行氧化反應形成糠酸(furoic acid,FAC),再將糠酸與鹼金族碳酸鹽進行羧基化反應形成FDCA的製程則給與合成FDCA新的發展方向。其中第一段反應是與法國CNRS學者Paul合作開發氧化反應生成糠酸, 使用DP法 (deposition precipitation)製備Au/HT氧化觸媒,此氧化觸媒在1%糠醛水溶液中加入6bar氧氣,在反應溫度110℃, 進行2小時反應可得到95%產率的糠酸。而後進行第二段的CO2羧基化反應,使用Cs2CO3 或是K / Cs混合的碳酸鹽為鹼性觸媒,可以合成78%的FDCA產物。其主要反應機構是(1)糠酸先與半熔態的鹼金族碳酸鹽反應形成糠酸鹽(furoic salt),同時脫除水份,注意水的移除可防止高溫下裂解反應而產生其它副產物的雜質,(2)糠酸鹽與碳酸鹽CO32-反應,在furan環上第5個碳上的氫原子進行C-H的脫質子反應,形成碳陰離子(carbanion)中間態,而Cs+離子在高溫下可以穩定此中間態,此時加入的CO2可以與碳陰離子進行C-C鍵加成的羧基化反應而形成FDCA 銫鹽化物,在單獨使用Cs碳酸鹽時,在260℃小量反應時可達89% FDCA鹽類產率。但增加原料反應量時,則產率會因其它副產物的生成而降至71%。(3)FDCA 鹽類與鹽酸進行質子酸化反應可得到FDCA及CsCl水溶液,(4)CsCl水溶液加入CO2及雙極膜的電化學反應,可以重新回收HCl及Cs碳酸鹽。連結此4段反應單元形成完整的循環鏈,可將價格較高的Cs2CO3 減少消耗量,持續進入循環再利用的製程。(圖八)
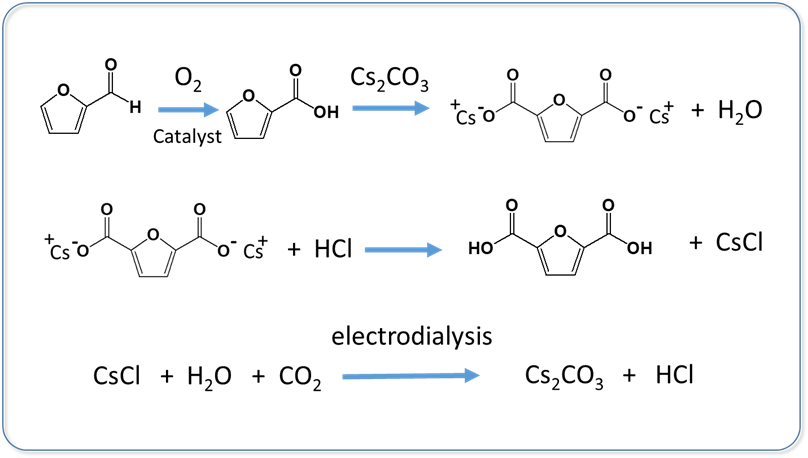
圖八、 糠酸與鹼性碳酸鹽製備FDCA單體的技術
此外Kanan教授更進一步的進行不同鹼性觸媒的反應測試。(1)使用不同的鹼金族碳酸鹽會有不同的效果。Kanan教授測試單獨使用Cs碳酸鹽,在260℃反應時即可達到71%FDCA的高產率。但如果全部改成K碳酸鹽,不論溫度高低,皆無法產生FDCA。其差異原因在於Cs在260℃即會有半熔化的結晶狀態,促進在較低溫度即達到高產率。而若是測試使用Cs及K 的碳酸鹽混合系統,則不會有大量熔化態出現,當K愈多(K/Cs=1/1 -4/1),反應溫度要愈高(275-290℃)才能有高產率。但相對的在高溫有機物也愈易裂解形成焦物、醋酸、丙二酸類雜質。(2)加入CO2對產物有穩定的效果。在285℃,K/Cs=2/1,在有CO2的保護下,其產率可達63%。在相同條件中,若不加CO2,改成使用氮氣,則大幅度的產率下降,增加大量裂解產物。
義大利Bari“ALDO MORO”巴里大學的Angela Dibenedetto教授測試多種碳酸鹽類與糠酸進行反應,當使用碳酸銫及糠酸在220℃,6MPa二氧化碳下,FDCA產率可達76%,若使用其團隊合成的Cu(FC)2做為原料,其產率可達99%。該研究的重點為(1)以Cu(OH)2合成Cu (furoate)2的錯合物分子(以下簡稱Cu(FC)2),由NMR證實在糠酸呋喃環上第5碳位置的氫原子是易於交換D2O,證實此氫原子位置是具有較強酸性而易被鹼性觸媒移除形成碳陰離子。而Cu(FG)2的NMR位置則更明顯位移,其分子內電子密度效應將呋喃環上第5個碳位置的氫原子更增加酸性,進而在鹼性觸媒催化下,易與CO2反應合成FDCA產物(圖九)。(2)使用Cu(FC)2及Cs2CO3/MgCO3的混合碳酸鹽催化系統,也可將FDCA產率增高到94%。 (3)使用糠酸甲酯化合物為原料,在Cs2CO3觸媒或是Cs2CO3/MgCO3觸媒的催化條件下,皆可以達到91%及88%的FDCA產率。(表四)
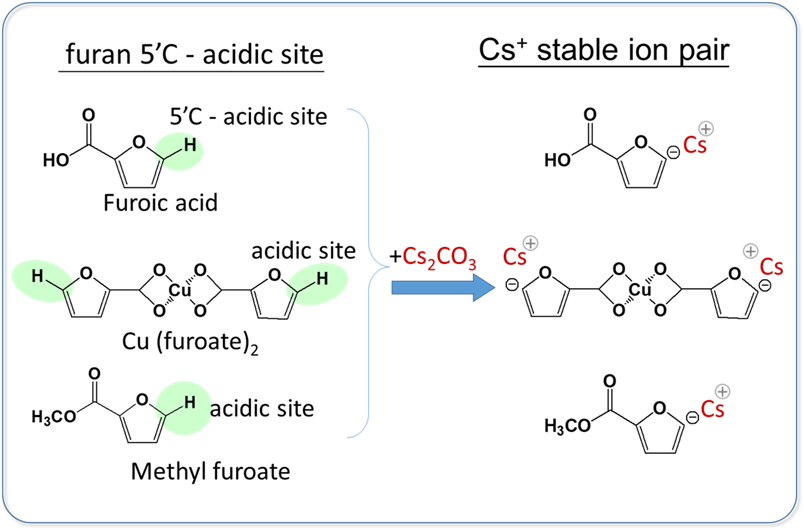
圖九、 糠酸及其衍生物以鹼性觸媒活化機制
表四、 糠酸衍生物合成FDCA
| 原料 | 觸媒 | 反應溫度(K) | 反應壓力 | 反應時間(hr) | FDCA產率(%) | 使用糠酸原料 FDCA產率(%) |
| Cu(FA)2 | Cs2CO3 | 493 | 6MPa, CO2 | 5 | 89 | 70 |
| Cs2CO3 | 493 | 6MPa, CO2 | 20 | 99 | 76 | |
| Cs2CO3 | 513 | 6MPa, CO2 | 20 | 97 | 75 | |
| Cs2CO3 | 493 | 6MPa, N2 | 20 | 93 | 75 | |
| Cs2CO3/ MgCO3 | 493 | 6MPa, CO2 | 20 | 94 | 69 | |
| 糠酸甲酯 | Cs2CO3 | 493 | 6MPa, CO2 | 5 | 46 | - |
| Cs2CO3 | 493 | 6MPa, CO2 | 20 | 91 | - | |
| Cs2CO3 | 493 | 6MPa, N2 | 20 | 62 | - | |
| Cs2CO3/ MgCO3 | 493 | 6MPa, CO2 | 20 | 88 | - |
Journal of CO₂ Utilization 32 (2019) 170–177
由上述的各項研究中,從半纖維素或木質纖維素裂解出的5碳糖生質原料可以轉化成糠醛後氧化生成糠酸,而糠酸或其衍生物Cu(FC)2及糠酸甲酯皆可在Cs2CO3觸媒或鹼性混合碳酸鹽Cs2CO3/K2CO3、Cs2CO3/MgCO3的催化下可以產生高產率的FDCA,此項技術開廣FDCA的原料來源,同時也在反應中使用CO2為原料,達到減少CO2的效用。
四、總結
全球新一代的觸媒技術已將CO2轉換成化學品的效率逐步提升。以CO2合成碳酸烷基酯類的化學品在新型CeO2、ZrO2、有機錫觸媒的發展下已逐漸進入試量產放大的技術。而以生質半纖維素來源的糠醛衍生物製造FDCA的觸媒技術開發,也使FDCA單體有新的製造技術。其開發方向都逐步朝向高效率催化、環境無害、低成本能耗等項目發展。後續開發新型CO2再利用的觸媒催化系統是需要持續發展的重要關鍵,若能有效應用於CO2循環應用化學材料產業,可符合全球溫室氣體減量的共識,並可推動國內發展高值低碳排放的循環經濟,強化國內下游產品的低碳排綠色競爭力。
參考資料
- Y. Yoshida, Y. Arai, S. Kado, K. Kunimori & K. Tomishige, “Direct synthesis of organic carbonates from the reaction of CO2 with methanol and ethanol over CeO2 catalysts”, Catalysis Today 115 (2006) 95–101.
- K. Tomishige, T. Sakaihori, Y. Ikeda & K. Fujimoto, “A novel method of direct synthesis of dimethyl carbonate from methanol and carbon dioxide catalyzed by zirconia”, Catalysis Letters 58 (1999) 225–229.
- M. Zhang, M. Xiao, S. Wang, D. Han, Y. Lu & Y. Men, “Cerium oxide-based catalysts made by template-precipitation for the dimethyl carbonate synthesis from carbon dioxide and methanol” , Journal of Cleaner Production 103 (2015) 847-853.
- K. Tomishige & K. Kunimori, “Catalytic and direct synthesis of dimethyl carbonate starting from carbon dioxide using CeO2-ZrO2 solid solution heterogeneous catalyst: effect of H2O removal from the reaction system”, Appl. Catal. A: General 237 (2002) 103-109.
- M. Honda, M. Tamura, Y. Nakagawa, K. Nakao, K. Suzuki & K. Tomishige, “Organic carbonate synthesis from CO2 and alcohol over CeO2 with 2-cyanopyridine: Scope and mechanistic studies”, Journal of Catalysis 318 (2014) 95-107.
- M. Honda, M. Tamura, Y. Nakagawa, S. Sonehara, K. Suzuki, K. Fujimoto & K. Tomishige, “Ceria‐catalyzed conversion of carbon dioxide into dimethyl carbonate with 2‐cyanopyridine”, ChemSusChem, 6 (2013) 1341-1344.
- A. Banerjee, G. R. Dick, T. Yoshino & M. W. Kanan, “Carbon dioxide utilization via carbonate-promoted C–H carboxylation”, Nature 531 (2016) 215-219.
- A. Banerjee, G. R. Dick, T. Yoshino & M. W. Kanan, “A scalable carboxylation route to furan-2,5- dicarboxylic acid”, Green Chem. 19 (2017) 2966-2972.
- F. Nocito, N. Ditaranto & A. Dibenedetto, “Valorization of C5 polyols by direct carboxylation to FDCA: Synthesis and characterization of a key intermediate and role of carbon dioxide”, Journal of CO₂ Utilization 32 (2019) 170-177.
- 點閱次數
- 3771
- 目前評價
- 5
- 評價
